Индуктивный эффект
Индуктивный эффект
Органические соединения образуются в результате обмена электронов между двумя или группой атомов. Движение (смещение) электронов под воздействием других видов. Это приводит к ряду эффектов,: Индуктивный эффект, Electromeric эффект, эффект сверхсопряжения, Резонансный эффект. Говоря в широком смысле, химическая реакция означает перенесение или обмен электронами происходит между атомами.
Что такое индуктивный эффект (я эффект) – Definition
Индуктивный эффект возникает в органических молекулах, когда некоторые атомы или группы разных электроотрицательность присоединен к атому углерода цепи. Ковалентная связь образуется при равном распределении электронов между двумя атомами.
- В случае ковалентной связи между двумя атомами аналогичных, электронная пара связи занимает центральное положение между ядрами двух атомов соответствующих. Такая ковалентная связь называется неполярной связью.
- С другой стороны, в случае ковалентной связи между двумя разнородными атомами, пара электронов, образующая связь никогда не разделяет абсолютно поровну между двумя атомами, но привлекает немного больше в стороне более электроотрицательного (свойство привлекающих электронов) атом.
Должен прочитать:
- Полярные и неполярные соединения.
- Примеры ковалентной связи.
| Постоянное смещение электронов вдоль цепи атомов углерода в связи с наличием атома или группы атомов различной электроотрицательности в конце цепочки. |
- Индуктивный эффект постоянный эффект.
- Она возникает из-за разницы электроотрицательных.
- Он действует на Е, связанного электрона.
Индукционные Примеры эффектов
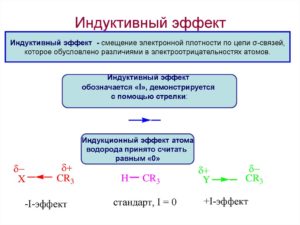
- Чтобы понять Индуктивный эффект хорошо давайте рассмотрим пример. В соединении C-X, где Х является более электроотрицательным, чем C, пара электронов, образующий С-X связь несколько больше привлекает к атому X, в результате последний достигает частичный отрицательный заряд (обозначается ? -) в то время как атом углерода достигает частичный положительный заряд (обозначается ?+).
- С другой стороны, в соединениях, таких как C-Y, где Y представляет собой электроположительный элемент или группа, то есть, С более электроотрицательным, чем Y, электронная пара формирования С-Y связь несколько смещен в сторону атома углерода и, следовательно, С и Y достигают частичные отрицательные и частичные положительные заряды, соответственно,.
- Хлор, имеющий большее значение электроотрицательности, чем carbon.This вызвать электронную пару между CA и Cl будет смещена в сторону атома хлора. следовательно, Cl приобретает небольшой отрицательный заряд, и СA получит небольшой положительный заряд. Так как CA заряжена положительно, он будет привлекать электронную пару, образующую ковалентную связь между CA и CВ.Это приведет к CВ будет также приобрести небольшой положительный заряд, но заряд на CВ будет меньше, чем на СA. В дальнейшем, эффект атома хлора (источник) был передан через CA в CВ чем CС. Этот эффект уменьшается с увеличением расстояния от электроотрицательного элемента.
+я Effect
Если атом или группа привлекает электроны менее сильно, чем водород, он, как говорят, + Я эффект (электрон отпугивания или электронно-рилизинг).
-я Effect
Любой атом или группа, если притягивает электроны сильнее, чем водород,, он сказал, чтобы иметь эффект -I (электрон-привлечение или электронно-акцепторный). Важные атомы или группы расположены ниже в порядке убывания.
| +я эффект | -Я Эффект |
| Электронно отпуская группа. | Электронно-акцепторные группы. |
| EN меньше, чем H. | Больший, чем H. |
| Те группы, которые показывают + I эффект рассеивается. | Группа показывает эффект -I рассеивает положительный заряд на C-цепи. |
Применение индуктивного эффекта
Явление индуктивного эффекта очень важно в органической химии, как она объясняет некоторые факты, наиболее важными из которых приведены здесь.
Реакционная способность алкилгалогенидов
галогениды алкильных(Р-Х), в целом, более активны, чем соответствующий алкан по той причине, присутствие С-Х в связи алкилгалогениды, благодаря которому они подвергаются индуктивный эффект.
Прочность карбоновых кислот
Кислота представляет собой вид, который имеет тенденцию терять протон. более того, сила кислоты зависит от легкости, с которой кислотный ионизирует, чтобы дать протон.
Таким образом, любая структурная единица, как сильно электроотрицательной группа, которая помогает в удалении протона от гидроксильной группы кислоты будет иметь эффект создания соответствующей карбоновую кислоты более сильный.
| Характеристика | -я | +я |
| Кислотные Природа | ↑ | ↓ |
| Основная Природа | ↓ | ↑ |
Основной характер аминов
Соединение называется основными по своей природе, если он способен принимать протон. Основной характер аминов обусловлена наличием неподеленной пары электронов на атоме азота, который принимает протон, готовность, с которой неподеленной пары электронов доступна для координации с протоном определяет относительную основную силу амины.
если вам нравится доля статьи с другими.
Индуктивное влияние фенильных групп на кислотность
Индуктивный эффект может выражаться в системе с пирамидальной конфигурацией карбаниона, закрепленной наличием мостиковой системы:
Рисунок 3.
Согласно шкале кислотности МСЭД для трифенилметана $pka=32,5$, для триптицена — $38$ и для метана — $40$.
У аниона триптицена ориентация орбиталей жестко закреплена, поэтому эффект делокализации заряда выражен незначительно. Индуктивное влияние в триптицене трех фенильных групп достаточно велико, чтобы вызвать увеличение кислотности около двух единиц по шкале МСЭД.
Индуктивный эффект и его взаимосвязь с эффектом сопряжения
Как правило, на стабилизацию карбанионов оказывают влияние факторы, которые состоят из суммы разных электронных эффектов. Чаще всего это индуктивный эффект и эффект сопряжения.
Многие ученые (Тафт, Кон и Джонс) пытались эти эффекты разделить. Они опирались на величины констант заместителей ($sigma $-), полученных из значений рКа ряда мета- и пара-замещенных фенолов в воде при $25circ C$.
Параметр ${sigma }-_n$ разделили на резонансную (${sigma }-_R$) и индуктивную (${sigma }-_I$) с использованием допущений:
Чем выше положительное значение $sigma $-, тем больше стабилизация заместителем аниона.В таблице показан относительный вклад индуктивного и резонансного эффектов в способность заместителя увеличивать кислотность фенолов:
Рисунок 4.
Отношение ${sigma }-_R$/${sigma }-_I$ для групп, способных к сопряжению ($CONH_2, CN, COOC_2H_5, CHO, COCH_3, NO_2$) колеблется:
- цианогруппа — $1,2$;
- ацетильная группа — $2,8$.
Индуктивный эффект вносит большой вклад в суммарный эффект заместителя, в том числе для групп, способных наилучшим образом вступать с отрицательным зарядом в сопряжение.
Взаимосвязь индуктивного эффекта с эффектами сопряжения объяснили кинетические исследования по скорости изотопного обмена, катализируемого основанием.
Были изучены скорости изотопного обмена между рядом монозамещеннных ацетиленов и $D_2O$ в диметилформамиде в присутствии триэтиламина.
Водород в качестве заместителя можно сравнить с фенилом, что указывает на незначительную величину, действующего в обратном направлении эффекта сопряжения, который стремится рассредоточить положительный заряд по бензольному кольцу.
Близость кинетической кислотности фенилацетилена и ацетилена сильно контрастирует с различием почти в шесть единиц по шкале МСЭД.
Рисунок 5.
Ни в одном из заместителей делокализация отрицательного заряда не сводилась просто к эффекту сопряжения. n-Метоксифенильная и фенильная группы действуют одинаково. Это указывает на то, что электронодонорные свойства метоксигруппы почти полностью убирают дополнительный индуктивный эффект, которым она обладает.
Если метоксигруппа находится в непосредственной близости с тройной связью, то она увеличивает скорость обмена по сравнению с ацетиленом в три раза.
Сравнение скоростей мета- и пара-галогенфенилацетиленов указывает на то, что эффект сопряжения электронных пар атомов галогена накладывается на их индуктивный эффект.
