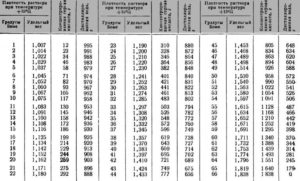
Плотность водных растворов плавиковой кислоты
Плавиковая кислота
плавиковая кислота, плавиковая кислота в стоматологии
Пла́виковая кислота́ (фтороводоро́дная кислота́, фтористоводоро́дная кислота́, гидрофторидная кислота́) — водный раствор фтороводорода (HF). Промышленностью выпускается в виде 40 % (чаще), а также 50 % и 72 % растворов.
Название «плавиковая кислота» происходит от плавикового шпата, из которого получают фтороводород.
- 1 Свойства
- 1.1 Физические
- 1.2 Химические
- 2 Техническая плавиковая кислота
- 3 Применение
- 4 Токсические свойства
- 5 Примечания
Физические
Бесцветная жидкость. Растворение фтористого водорода в воде сопровождается довольно значительным выделением тепла (59,1 кДж/моль). Для него характерно образование содержащей 38,3 % HF и кипящей при 112 °C азеотропной смеси (по другим данным 37,5 % и tкип 109 °C). Такая азеотропная смесь получается в конечном счёте при перегонке как концентрированной, так и разбавленной кислоты.
При низких температурах фтористый водород образует нестойкие соединения с водой состава Н2О·HF, Н2О·2HF и Н2О·4HF. Наиболее устойчиво из них первое (tпл −35 °C), которое следует рассматривать как фторид гидроксония — F. Второе является гидрофторидом гидроксония .
Химические
Плавиковая кислота — кислота средней силы (константа диссоциации составляет 6,8·10−4, степень диссоциации 0,1 н. раствора 9 %). Она разъедает стекло и другие силикатные материалы, поэтому плавиковую кислоту хранят и транспортируют в полиэтиленовой таре.
Реакция идёт с выделением газообразного фторида кремния (SiF4):
.
Реагирует со многими металлами с образованием фторидов (свинец не растворяется в плавиковой кислоте, так как на его поверхности образуется нерастворимый фторид PbF2; платина, палладий и золото также не растворяются), не действует на парафин, который используют при хранении этой кислоты.
Техническая плавиковая кислота
Техническая плавиковая кислота обычно содержит ряд примесей — Fe, Rb, As, кремнефтористоводородную кислоту Н2SiF6, SO2 и др.
Для грубой очистки её перегоняют в аппаратах из платины или свинца, отбрасывая первые порции дистиллята.
Для получения более чистой кислоты техническую кислоту переводят в гидродифторид калия, затем разлагают его нагреванием, растворяя фтористый водород в дистиллированной воде.Крепкая плавиковая кислота (более 60 % HF) может сохраняться и транспортироваться в стальных ёмкостях. Для хранения плавиковой кислоты и работы с ней в лабораторных условиях наиболее удобны сосуды из тефлона, полиэтилена и других пластмасс.
Применение
Крупный потребитель фтороводородной кислоты — алюминиевая промышленность.
- Раствор фтороводорода применяется для прозрачного травления силикатного стекла (например — нанесение надписей — для этого стекло покрывают парафином, прорезая отверстия для травления). Матовое травление получают в парах фтороводорода.
- Для травления кремния в полупроводниковой промышленности.
- В составе травильных, травильно-полировальных смесей, растворов для электрохимической обработки нержавеющей стали и специальных сплавов.
- Получение фторидов, кремнефторидов и борфторидов, фторорганических соединений, а также соответствующих кислот (кремнефтороводородная кислота и борфтороводородная кислота), синтетических смазочных масел и пластических масс.
- Для растворения силикатов при различного рода анализах.
- В процессе алкилирования, в качестве катализатора в реакции изобутана и олефина.
Токсические свойства
Плавиковая кислота ядовита. Обладает слабым наркотическим действием. Возможны острые и хронические отравления с изменением крови и кроветворных органов, органов пищеварительной системы, отёк лёгких.
Обладает выраженным эффектом при вдыхании, раздражающим действием на кожу и слизистые оболочки глаз (вызывает болезненные ожоги и изъязвления); кожно-резорбтивным, эмбриотропным, мутагенным и кумулятивным действием. Ей присвоен второй класс опасности для окружающей среды, в то время, как чистый фтороводород принадлежит к первому классу опасности.
При попадании на кожу в первый момент не вызывает сильной боли, легко и незаметно всасывается, но через короткое время вызывает отёк, боль, химический ожог и общетоксическое действие. Симптомы от воздействия слабо концентрированных растворов могут появиться через сутки и даже более после попадания их на кожу.
При попадании в кровь через кожу связывает кальций крови и может вызвать нарушение сердечной деятельности. Ожоги площадью более чем 160 см2 опасны возможными системными токсическими проявлениями.
Токсичность плавиковой кислоты и её растворимых солей предположительно объясняется способностью свободных ионов фтора связывать биологически важные ионы кальция и магния в нерастворимые соли (см. Отравление фторидами (англ.)).
Поэтому для лечения последствий воздействия плавиковой кислоты часто используют глюконат кальция, как источник ионов Ca2+. Пострадавшие участки при ожогах плавиковой кислотой промываются водой и обрабатываются 2,5 % гелем глюконата кальция.
Тем не менее, поскольку кислота проникает сквозь кожу, простого промывания недостаточно и необходимо обращение к врачу для проведения лечения. Высокую эффективность показали внутриартериальные инфузии хлорида кальция.
Предельно допустимая концентрация (ПДК) плавиковой кислоты:
| ПДК в воздухе рабочей зоны, мг/м³ (в пересчёте на фтор) | 0,5 | 0,1 |
| ПДК в атмосферном воздухе, мг/м³ (в пересчёте на фтор) | 0,02 | 0,005 |
Примечания
- ↑ Исконный произносительный вариант «плавико́вая», зафиксированный в словарях XIX (например, в словаре В. И. Даля) и первой половины XX века, устарел.
- ↑ Растворение стекла в плавиковой кислоте — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ ГОСТ 12.1.007-76 — Система стандартов безопасности труда. Вредные вещества
- ↑ el Saadi MS, Hall AH, Hall PK, Riggs BS, Augenstein WL, Rumack BH (1989).
«Hydrofluoric acid dermal exposure». Vet Hum Toxicol 31 (3): 243–7. PMID 2741315.
- ↑ Roblin I, Urban M, Flicoteau D, Martin C, Pradeau D (2006). «Topical treatment of experimental hydrofluoric acid skin burns by 2.5% calcium gluconate». J Burn Care Res 27 (6): 889–94. DOI:10.
1097/01.BCR.0000245767.54278.09. PMID 17091088.
- ↑ Recommended Medical Treatment for Hydrofluoric Acid Exposure (PDF). Honeywell Specialty Materials. Проверено 6 мая 2009. Архивировано из первоисточника 2 февраля 2012.
- ↑ Intra-arterial calcium infusion for hydrofluoric acid burns.
NCBI. Проверено 3 января 2010.
плавиковая кислота, плавиковая кислота в стоматологии, плавиковая кислота купить, плавиковая кислота формула
Плавиковая кислота Информацию О
Плавиковая кислота
Плавиковая кислота
Плавиковая кислота Вы просматриваете субъект
Плавиковая кислота что, Плавиковая кислота кто, Плавиковая кислота описание
There are excerpts from wikipedia on this article and video
Наш сайт имеет систему в функции поисковой системы. Выше: «что вы искали?»вы можете запросить все в системе с коробкой. Добро пожаловать в нашу простую, стильную и быструю поисковую систему, которую мы подготовили, чтобы предоставить вам самую точную и актуальную информацию.
Поисковая система, разработанная для вас, доставляет вам самую актуальную и точную информацию с простым дизайном и системой быстрого функционирования. Вы можете найти почти любую информацию, которую вы ищете на нашем сайте.
На данный момент мы служим только на английском, турецком, русском, украинском, казахском и белорусском языках.
Очень скоро в систему будут добавлены новые языки.
Свойства и применение плавиковой кислоты

Плавиковая кислота (фтороводородная/фтористоводородная/гидрофторидная кислота) – это вещество неорганической этимологии, раствор гидрофторида в воде, 1-основная кислота.
Промышленный выпуск осуществляется в разных концентрациях: 40 % (наиболее распространенный вариант), 50 % и 72 %.
Наименование веществу дал плавиковый шпат – сырье для получения рассматриваемой кислоты.
Молярная масса – 20,0063 г/моль, плотность – 1,15 г/см³. Термосвойства: t плавления – -83,55 °C, t кипения – 85,8 °C. Формула: HF.
Свойства плавиковой кислоты
Физические. Это жидкий не имеющий окраса легкоподвижный материал. Запах – острый, обжигающий. При сочетании с водой смешивается.
Растворение фтороводорода в воде приводит к возникновению весьма большого количества тепла (59,1 кДж/моль). Получается продукт с 38,6 % (37,5 %) HF, азеотропная смесь, которая кипит при 114 °C (109 °C).
Он является результатом работы как с высококонцентрированным, так и с разбавленным веществом.
Небольшие температурные параметры – предусловие формирования соединений, не отличающихся стойкостью, при контакте гидрофторида и воды.
Химические. Гидрофторидная кислота принадлежит к средне сильным кислотам.
Она способна разъедать стекло и прочие силикаты (это единственная кислота, реагирующая с оксидом кремния – основой всех силикатных материалов), поэтому хранение и перевозку нужно осуществлять в ПЭ таре, ни в коем случае не в стеклянных емкостях. Реакция протекает с выделением фторида кремния в газообразном состоянии.
Плавиковая кислота реагирует с различными металлами, при этом формируются фториды. Растворению в ней не поддаются свинец, платина, золото и палладий. Отсутствует ее влияние и на такие материалы, как парафин, каучук, полиэтилен, фторопласт и прочие пластики. Если ее концентрация не превышает 60 %, то воздействия не происходит и на железо.
Еще одно интересное свойство данного вещества заключается в замерзании воды при более низкой t, если внести в нее HF.
Токсические. Фтороводородная кислота не горючая, но осуществляет сильное токсическое влияние на людей и окружающую среду. Она не только ядовита, но и характеризуется наркотическим воздействием.
Может стать причиной острых отравлений, внести негативные изменения в пищеварительный тракт, кровь и органы кроветворения, а также привести к отеку легких.
Проникнув в кровь сквозь кожу, может связывать кальций и нарушать деятельность сердечно-сосудистой системы.
Чревата пагубными последствиями при вдыхании, раздражением кожных покровов и слизистых оболочек, обладает кожно-резорбтивной и эмбриотоксичностью, имеет мутагенное действие и способна накапливаться в организме.
Сама кислота, как и чистый фтороводород, принадлежит ко 2-му классу опасности по воздействию на внешнюю среду.Нужно соблюдать осторожность, так как при начальном контакте с кожей фтористоводородная кислота может не вызывать обильных болевых ощущений, продолжая при этом потихоньку и незаметно всасываться. Но пройдет некоторое время – и во всей силе проявят себя химические ожоги, боли, отеки и общий токсический эффект.
Плавиковая кислота: применение
Высокочистый и технический материал различных концентраций находит применение во многих отраслях. Основные из них следующие:
– стекольное производство (прозрачное травление кремниевого стекла, удаление шероховатости из поверхности хрусталя);
– нефтехимия и горнодобывающее направление (обработка и очистка поверхностей, увеличение эффективности добычи нефти путем изъятия асфальтовых и парафиновых отложений, разрушение пород, содержащих кремний);
– химия (выделение ряда металлов, в частности Ta, Zr и Nb, катализ некоторых хим. процессов, в частности при алкилировании в реакции изобутана и олефина, а также изготовление фторлонов, холодильных агентов, содержащих фтор кислот, боратов и фторидов, орган. соединений на основе F, искусственных смазок и пластмасс);
– аналитическая химия (растворение силикатных соединений);
– алюминиевая промышленность (изготовление алюминия электролитическим методом и работа с ним);
– металлообработка (входит в состав композиций, предназначенных для травления и полирования, электрохим. обработки сплавов и нержавейки, используется при очищении заготовок из металла от песка и керамических примесей);
– полупроводниковая отрасль (очищение и травление кремния для полупроводников);
– стоматология и зуботехническое дело (изъятие с внутренней стороны протезов из керамики лейцита, плюс выступает протравливающим веществом и элементом металлического каркаса под керамические коронки, обеспечивающим надежную фиксацию);
– создание фильтровальных систем.
Как видите, несмотря на свою опасность, плавиковая кислота ввиду ряда ценных физических и химических свойств очень важна для разных отраслей. Используйте ее с учетом всех требований безопасности – сведете к минимуму негативные последствия, получив при этом желаемые результаты работы.
Кислота фтористоводородная 40%

Плавиковая кислота является водным раствором газообразного фтороводорода (HF). Представляет собой сильнейшее по степени разрушения минеральное соединение. В силу специфических свойств широко используется в различных производственных и лабораторных целях. Требует особых условий при транспортировке, хранении и работе. У нас в наличии фтористоводородная кислота 40%.
Купить от 1 канистры 33,5 кг по цене, в которую входит НДС
Стоимость может корректироваться индивидуально для каждого клиента.
В наличии на складе. Предоплата, отсрочка платежа, оплата по факту поступления материала на склад покупателя.
Доставка: по городу – бесплатно от 500 кг. По всей России транспортными компаниями.
Самовывоз: г. Челябинск, ул. Механическая 14.
Канистры 30 л (33,5 кг) и еврокуб (1000 л)
Доставка в автоцистернах и жд-цистернах транспортными компаниями
Плавиковая кислота
В химии называется фтористоводородной или плавиковой кислотой, а также гидрофторидной, поскольку в процессе ее производства используется плавиковый шпат. Этот минерал относится к флюоритам (содержащим фтор) и имеет свойство свечения в ультрафиолетовых лучах или при температурном воздействии.
Мы также продаем лимоннуюн и ортофосфорную термическую.
Физические свойства
При обычных условиях окружающей среды фтороводородная кислота предстает в виде прозрачной бесцветной жидкости с резким удушливым запахом фтористого водорода. Плотность раствора — 1,2 г/дм3. Не проявляет горючие, пожаро и взрывоопасные свойства. Понижает температуру замерзания воды даже в сильноразбавленных растворах.
Химические свойства фтористоводородной кислоты
В химическом отношении проявляет себя как кислота средней силы:
- взаимодействует практически со всеми металлами с образованием солей (фторидов);
- растворяет стекло, поскольку вступает в реакцию с оксидом кремния и образует силикаты;
- не вступает в реакцию со свинцом, золотом и металлами платиновой группы;
- концентрированный раствор (больше 60%) не реагирует с железом;
- не разрушает изделия из парафина, фторопласта, каучука, пластмасс.
Применение плавиковой кислоты
Фтороводородная кислота производится в виде растворов разной концентрации, степени чистоты (с высокой степенью чистоты или техническая с микропримесями). Находит применение в различных сферах и отраслях:
- аналитической химии – в процессах пробоподготовки труднорастворимых образцов;
- стекольной отрасли – в качестве реагента для травления изделий из кремниевого стекла;
- металлургии – при выделении редких металлов (циркония, ниобия, тантала и др.);
- электронике – травление и обработка кремния в полупроводниках;
- химической промышленности – как катализатор процессов производства минеральных солей, хладагентов, фторопластов, смазочных масел, при получении алюминия;
- нефтехимии и горнорудном деле – разрушение кремнийсодержащих пород, углубление скважин и чистка аппаратуры от углеводородных отложений;
- электрохимии – в качестве средства для полировки, травления, чистки поверхностей и изделий из сплавов, нержавеющей стали от песка и загрязнений;
- в качестве средства для химической полировки керамических, хрустальных изделий – удаления с их поверхности шероховатостей и дефектов.
Особенности перевозки и хранения
В силу высокой разрушительной способности плавиковую кислоту транспортируют в емкостях (контейнерах, кубах, канистрах), изготовленных из фторопласта или полиэтилена. Большие емкости обязательно укладываются в корпус из металлической обрешетки.
Транспортировка осуществляется железнодорожным способом или автомобильным транспортом с использованием стальных и железных цистерн. Строго запрещен налив в стеклянную тару, которая растворяется едким реагентом.
Токсичность и вредное воздействие
Фтороводородную кислоту относят ко 2-му классу по вредности воздействия на человека. Ее раствор трудно отличить от обычной воды, что создает угрозу случайного заглатывания. Вещество способно проникать в кровоток и вызывать токсическое действие:
- отек легких, удушье;
- нарушение сердечной деятельности;
- проблемы с желудочно-кишечным трактом;
- легкий наркотический эффект;
- повреждение молекул ДНК.
При попадании фтористоводороной кислоты на кожные покровы наблюдается химический ожог в виде отеков тканей и глубоких долгозаживающих язв. Бесцветный фтористый водород в газообразном состоянии – сильнейший яд, который относится к 1-му токсикологическому классу. Едкое вещество раздражает слизистые ткани дыхательных путей, глаз.
Меры безопасности
Любые работы с плавиковой кислотой производятся в вытяжных шкафах при включенной вентиляции. Рабочий персонал обеспечивается спецодеждой, защитными очками, резиновыми перчатками и противогазами с автономной подачей воздуха.
При попадании реактива на кожу необходимо промыть пораженное место обильным количеством воды, после чего обработать участок составом с глюконатом кальция. Пострадавшего срочно госпитализируют, где в качестве антидота используют хлорид кальция в виде внутривенных вливаний.
Физические[ | ]
Бесцветная легкоподвижная жидкость с резким запахом и обжигающим «уксусным» вкусом. Растворение фтористого водорода в воде сопровождается довольно значительным выделением тепла (59,1 кДж/моль).
Для него характерно образование содержащей 38,6 % HF и кипящей при 114 °C азеотропной смеси (по другим данным 37,5 % и tкип 109 °C).
Такая азеотропная смесь получается в конечном счёте при перегонке как концентрированной, так и разбавленной кислоты.
При низких температурах фтористый водород образует нестойкие соединения с водой состава Н2О·HF, Н2О·2HF и Н2О·4HF. Наиболее устойчиво из них первое (tпл −35 °C), которое следует рассматривать как фторид гидроксония — [Н3O]F. Второе является гидрофторидом гидроксония [Н3O][HF2].
Химические[ | ]
Плавиковая кислота — кислота довольно слабая (средней силы) (константа диссоциации составляет 6,8⋅10−4, степень диссоциации 0,1 н. раствора 9 %). Она разъедает стекло[2] и другие , поэтому плавиковую кислоту хранят и транспортируют в полиэтиленовой таре.
Реакция идёт с выделением газообразного фторида кремния (SiF4):
N a 2 O ⋅ C a O ⋅ 6 S i O 2 + 28 H F → N a 2 S i F 6 + C a S i F 6 + 4 S i F 4 ↑ + 14 H 2 O {displaystyle {mathsf {Na_{2}Ocdot CaOcdot 6SiO_{2}+28HF
ightarrow Na_{2}SiF_{6}+CaSiF_{6}+4SiF_{4}uparrow +14H_{2}O}}} .
Реагирует со многими металлами с образованием фторидов (свинец не растворяется в плавиковой кислоте, так как на его поверхности образуется нерастворимый фторид PbF2; платина, палладий и золото также не растворяются), не действует на парафин, который используют при хранении этой кислоты.
Техническая плавиковая кислота[ | ]
Техническая плавиковая кислота обычно содержит ряд примесей — Fe, Rb, As, кремнефтористоводородную кислоту Н2SiF6, SO2 и др.
Для грубой очистки её перегоняют в аппаратах из платины или свинца, отбрасывая первые порции дистиллята.
Для получения более чистой кислоты техническую кислоту переводят в гидрофторид калия, затем разлагают его нагреванием, растворяя фтористый водород в дистиллированной воде.Крепкая плавиковая кислота (более 60 % HF) может сохраняться и транспортироваться в стальных ёмкостях, но разъедает стекло. Для хранения плавиковой кислоты и работы с ней в лабораторных условиях требуются сосуды из тефлона, полиэтилена и других пластмасс.
Применение[ | ]
Крупный потребитель фтороводородной кислоты — алюминиевая промышленность.
Токсические свойства[ | ]
Плавиковая кислота ядовита. Возможны острые и хронические отравления с изменением крови и кроветворных органов, органов пищеварительной системы, отёк лёгких.
Обладает выраженным эффектом при вдыхании, раздражающим действием на кожу и слизистые оболочки глаз (вызывает болезненные ожоги и изъязвления); кожно-резорбтивным, эмбриотропным, мутагенным и . Ей присвоен второй класс опасности для окружающей среды; чистый фтороводород также принадлежит ко второму классу опасности[3].
При попадании на кожу в первый момент не вызывает сильной боли, легко и незаметно всасывается, но через короткое время вызывает отёк, боль, и общетоксическое действие. Симптомы от воздействия слабо концентрированных растворов могут появиться через сутки и даже более после попадания их на кожу.
При попадании в кровь через кожу связывает кальций крови и может вызвать нарушение сердечной деятельности. Ожоги площадью более чем 160 см2 опасны возможными системными токсическими проявлениями.
Токсичность плавиковой кислоты и её растворимых солей предположительно объясняется способностью свободных ионов фтора связывать биологически важные ионы кальция и магния в нерастворимые соли ([en]). Поэтому для лечения последствий воздействия плавиковой кислоты часто используют глюконат кальция, как источник ионов Ca2+.
Пострадавшие участки при ожогах плавиковой кислотой промываются водой и обрабатываются 2,5 % гелем глюконата кальция[4][5]. Тем не менее, поскольку кислота проникает сквозь кожу, простого промывания недостаточно и необходимо обращение к врачу для проведения лечения[6].
Высокую эффективность показали внутриартериальные инфузии хлорида кальция[7].
Предельно допустимая концентрация (ПДК) плавиковой кислоты:
| ПДК в воздухе рабочей зоны, мг/м³ (в пересчёте на фтор) | 0,5 | 0,1 |
| ПДК в атмосферном воздухе, мг/м³ (в пересчёте на фтор) | 0,02 | 0,005 |
Примечания[ | ]
- ↑ Исконный произносительный вариант «плавико́вая», зафиксированный в словарях XIX (например, в словаре В. И. Даля) и первой половины XX века, устарел.
- ↑ Растворение стекла в плавиковой кислоте — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ ГОСТ 14022-88— Водород фтористый безводный
- ↑ el Saadi MS, Hall AH, Hall PK, Riggs BS, Augenstein WL, Rumack BH (1989). “Hydrofluoric acid dermal exposure”. Vet Hum Toxicol. 31 (3): 243—7. PMID 2741315.
- ↑ Roblin I, Urban M, Flicoteau D, Martin C, Pradeau D (2006). “Topical treatment of experimental hydrofluoric acid skin burns by 2.5% calcium gluconate”. J Burn Care Res. 27 (6): 889—94. DOI:10.1097/01.BCR.0000245767.54278.09. PMID 17091088.
- ↑ Recommended Medical Treatment for Hydrofluoric Acid Exposure (PDF).
Honeywell Specialty Materials. Проверено 6 мая 2009. Архивировано 2 февраля 2012 года.
- ↑ Intra-arterial calcium infusion for hydrofluoric acid burns. NCBI. Проверено 3 января 2010.

